ホーム > 関連施設・センター > 研究力向上支援センター > 若きトップサイエンティストの挑戦 > vol11 田中達英先生(解剖学第二講座 講師)
ここから本文です。
vol11 【特別編】田中達英先生(解剖学第二講座 講師)
Research Story, vol.11【特別編】
奈良県立医科大学 解剖学第二講座 講師 田中達英先生
【Nature Immunology】2023年 3月,vol. 146(19),1425―1433

論文タイトル:
Dermal macrophages set pain sensitivity by modulating the amount of tissue NGF through an SNX25-Nrf2 pathway
皮膚マクロファージは組織NGFレベルをSNX25-NRF2経路によって制御し、痛みの感度を調節する
当コーナーは、奈良県立医科大学の助教・医員の先生方へのインタビューを主に掲載しておりますが、今回は、特別編と題して解剖学第二講座 講師の田中達英先生のインタビューをご紹介いたします。
2023年3月号(2023年1月26日オンライン版)のNature Immunology(IF=31.250、2021年度)に田中先生の論文が掲載されました。Nature Immunologyは免疫学分野の最高峰の1つに挙げられるNatureの姉妹誌です。今回は論文の内容をお伺いすると同時に、発表に至る裏話や今後の抱負などをお聞きしてきました。
➀今回の論文の骨子について専門領域以外の方でも理解できるようにご紹介いただけますか。
→人間は様々な痛みを感じます。痛みは嫌なものですが、この感覚があるからこそ人は日常生活を送ることができます。例えば、まれな病気で難病にも指定されている先天性無痛無汗症では痛みを感じることが出来ず、骨折・脱臼などの外傷や、自分で指先、舌・口唇をかんで傷つけてしまう行為を繰り返し、日常生活に困難をきたします。また、がんなど多くの疾患に伴う痛みをコントロールすることは治療のひとつとして重要です。痛みを感じるしくみについて、その伝達経路はよく調べられています。例えば皮膚に加わる痛みの場合、脊髄から伸びた皮膚直下の神経終末に刺激が入ると電気信号が脊髄を介して脳に到達し、最終的に大脳皮質の一次体性感覚野で痛みの情報が処理されます。しかし、この痛みという感覚を神経細胞がどのように感じているのかというメカニズムについてはまだまだわからないことばかりです。今回我々は、痛みについて偶然をきっかけに大きな発見をすることができました。それは、これまで想定されていなかった免疫細胞の1つであるマクロファージが痛みの制御に関与するというものでした。皮膚直下で神経細胞と密着するマクロファージは神経成長因子(NGF)という物質を分泌し、このNGF量が神経細胞に作用し痛みへの感度を決定している分子的要因であることを突き止めました。今回の発見は、様々な痛みに共通する根本的なメカニズムの理解につながると共に、痛みを抑える新たな薬の開発にもつながると期待しています。

(田中先生)
この研究の始まりは約10年前に遡ります。当研究室の辰巳晃子准教授が、脳のアストロサイト(日本語では星状膠細胞。多数の突起をもち「星のような」形態をした細胞で、脳内で神経細胞よりも数が多い。)の研究材料として使っていたトランスジェニック(TG)マウスが痛みに鈍感になっていることに気づかれました。このTGマウスは、機械刺激といった正常時の痛みから炎症のような病態時の痛みに対しても広く鈍感になっていました。この表現型の同定がきっかけとなり、本格的な痛み研究をスタートしました。奥田洋明助教(現、金沢大学准教授)がその後の3年間で、この表現型の原因遺伝子を突き止められました。もともとこのTGマウスはアストロサイトで発現するMlc1遺伝子をコントロールできるよう遺伝子操作した動物として研究されていたのですが、驚いたことに疼痛鈍麻の表現型にこのMlc1遺伝子は関係ないことがわかりました。奥田先生がさらに詳しく調べてみると、このTGマウスではMlc1遺伝子近傍にあるいくつかの遺伝子が壊れており、そのうちの1つであるSorting Nexin 25(SNX25)が疼痛鈍麻の原因遺伝子であることを突き止めました。SNX25は分子の細胞内輸送にかかわる機能が知られていましたが、痛みの感覚にどのような役割をもつかは想像できませんでした。
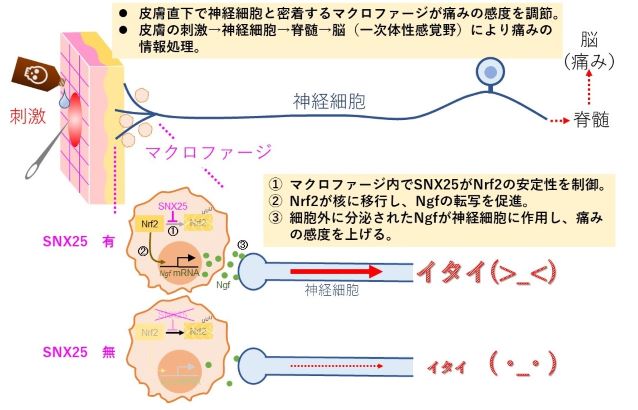
図.SNX25による新たな痛みの制御機構
奥田先生の転出に伴い、次に研究のバトンを私が引き継ぎ、7年かけてTGマウスが示す疼痛鈍麻の表現型の全容を明らかにできました。まず、私はSNX25遺伝子を神経細胞において特異的に破壊した遺伝子組み換えマウスを作製し調べてみました。しかし、SNX25が神経細胞で機能するという私の予想に反して疼痛鈍麻の表現型を示しませんでした。ここで早速壁に突き当たったのですが、出席した学会で骨髄移植と痛みに関する発表を聞き、神経ではなく骨髄由来の免疫系細胞が関与しているのではないかというアイデアがひらめきました。そこで研究室に戻り、すぐに骨髄移植の実験を試みました。細胞が緑色に光るGFPマウスから骨髄細胞をとりだし野生型マウスに移植したところ、皮膚の神経細胞近くに光る細胞を確認しました。皮膚の真皮層に移動し神経細胞に密着するような性質を持つ細胞として免疫細胞の1つマクロファージに着目しました。SNX25遺伝子をマクロファージ特異的に破壊した遺伝子組み換えマウスを作製したところ、見事に疼痛鈍麻の表現型を示しました。様々な追加実験からもSNX25に由来する疼痛がマクロファージを起点にしていることを確認しました。この結果を見て、今回の研究の視界がすっと開けた気がしました。和中明生教授の励ましもあり、よりインパクトのある成果を目指し、更に踏み込んで疼痛の発生メカニズムを解析しました。その結果、マクロファージ内でSNX25は転写因子であるNrf2タンパク質の安定性を制御することで、NGFの産生量を転写レベルで調節していることがわかりました。マクロファージから分泌されたNGFが神経細胞に作用し、痛みの感度を調節していたのです。このような感度調節は、疾患による痛みのみならず日常生活で感じる様々な痛みに共通する根本的なメカニズムではないかと考えています。
②【Nature Immunology】に論文が掲載されることになった評価ポイントについて、ご自身はどのような分析をしておられるでしょうか。
→生き物の表現型から原因となる遺伝子を同定する手法は順遺伝学と言います。今回偶然に見出したマウスの疼痛鈍麻の表現型から原因遺伝子を同定し、さらに踏み込んで痛みの分子メカニズに関して新しい発見が出来ました。このように順遺伝学的解析がほぼ完璧に進んだ点が評価されたのではないでしょうか。今回の研究では、免疫細胞の1つであるマクロファージが痛みの制御に重要な役割を持つことを発見しました。マクロファージは死んだ細胞や細菌の除去など体内の異物排除に働く機能が知られていましたが、痛みへの関与は全く想定されておらず、驚きの発見となりました。
もう1つの大きな発見は、痛みの感度が生理的な状態から調節されているということです。これまで痛みの研究は炎症などの疾患モデルを使って進められており、病気に伴う痛みのメカニズムは少しずつわかってきていました。一方、今回の研究で生理的な状態から痛みの感度が調節されているという新しい概念を導き出すことができました。痛みには個人差や男女間の性差があることが知られています。このような差が出る分子基盤は今回明らかにしたマクロファージから分泌されたNGFによる神経細胞の影響なのかもしれません。

(インタビューの様子)
➂今回の研究で特に苦労されたことがあれば教えてください。
→本研究では仮説の検証のために多くの遺伝子組み換えマウスを使う必要がありました。この作製に多くの時間がかかり、苦労しました。作製したマウスを使った実験が予想に反した結果になると、また新しいマウスを作製しなければなりません。時間との戦いの中で落ち込むこともありましたが、予想に反した結果だったからこそ、これまで誰も気づいていなかった大きな発見につながったともいえます。今となればよかったと思えます。
もう1つ苦労したのは、Nature Immunology誌でのリバイズです。リバイズとは査読者のアドバイスに従って論文を改訂し、科学的により信頼性を高める作業です。今回リバイズは大きく2回あり、約1年を要しました。1回目、2回目どちらもフローサイトメーターを使った膨大な量の追加実験を要求され、正直できるかどうか不安でした。共著者である石西綾美助教の頑張りにより何とか応えることができ、ほっとしました。2回のリバイズ後、論文の査読者には改訂版の内容で納得してもらえたのですが、雑誌の編集者から最終的な受理には図の大幅な再編成が必要で、それを1週間で対応するように要請されました。この1週間は本当に大変で、講座スタッフ総出で対応し、和中教授も研究室に泊まり込みで協力していただきました。編集者から論文受理の連絡が来た時は、講座所属員全員で歓喜の声を上げることができました。

(田中先生)
④この研究を始められた動機、またこの分野を専攻された経緯についてお聞かせください。
→大学を卒業し企業に就職したのですが、基礎研究をしたいと思い大学院進学を決意しました。大学院では、免疫細胞の研究により学位を取得しました。その後、旭川医科大学では脳のミクログリアという細胞の役割を動物モデルを使って研究しました。解剖学第二講座では脳のグリア細胞の研究をしていた関係で、助教として赴任することとなりました。こうして振り返ってみると、一貫して免疫細胞の役割を研究してきたことになります。
⑤田中先生はどのように苦労を乗り切ってこられたのでしょうか。
→今回の論文は、私の主要テーマとして奈良医大に赴任以来7年をかけて続けてきた研究成果です。7年という時間は長かったですが、これ以外にも複数のサブテーマを並行して研究していました。そちらの成果を論文発表できていた事は、研究者として成果が必要というプレッシャーを和らげ、精神衛生上よかったと思います。また、学部学生の研究を指導する機会に恵まれ、その成果を学生の筆頭論文として発表できました。大学の教育者として、研究の苦労も忘れさせてくれる程の大きな満足感を得ることが出来ました。
⑥今後の先生の目標についてお伺いします。研究内容等について差し支えない範囲でお話いただけますでしょうか。
→現在、2つのことに興味をもっています。1つは、痛み以外の体性感覚、例えば、触覚やかゆみでも、今回我々が見つけた神経に密着したマクロファージのような免疫細胞がその感度を調節しているのではないかと考えています。体性感覚固有のメカニズムに加え、我々が痛みで見出したメカニズムが共通に働いているのではないかと、興味を持っています。
2つ目は内臓痛です。今回の研究をしている中で、皮膚以外にも内臓粘膜固有層にある神経細胞にマクロファージが密着していることを見出しています。皮膚での痛み同様内臓痛において同様のメカニズムが働いている可能性が高いのではないかと興味をもっています。
⑦最後に、本研究を進めるにあたって多くの方々のご協力があったと思いますが、特に感謝をお伝えしたい方があればお聞かせください。
→一番はやはり今回の論文の共著者である当研究室の疼痛研究チームのメンバーです。まず、今回のチームを率いてきた解剖学第二講座の和中明生教授に感謝します。よりインパクトのある成果として発表できるように、じっくりと腰を据えた研究をさせていただきました。研究費のことは気にせず、どんどん進めて欲しいとお言葉を頂き、研究が佳境に入ると技術員の萬砂美都子さんに参画いただきました。また、今回の研究はTGマウスの表現型に気づかれた辰巳晃子准教授がいなければスタートしませんでした。奥田洋明金沢大学准教授には遺伝学的基盤を明らかにして研究のバトンを渡していただきました。今回の研究では、リバイズが本当に大変で約1年間かかりました。査読者からフローサイトメーターを用いた多くの追加データの要求があり、石西綾美助教が精力的な対応をしてくださいました。また、フローサイトメーターを用いた免疫細胞の実験では本学免疫学教室の伊藤利洋教授、北畠正大講師にお世話になりました。このような専門家が身近にいる本学の基礎研究力の高い環境が、Nature Immunologyというハイインパクトの学術誌への掲載につながったのではないかと考えています。

以上
<インタビュー後記>
今回お話をお伺いし、仲間を大切にされる先生との印象を持ちました。研究チームの全てのメンバーに感謝を忘れない先生の謙虚さが、この人を支えようという人望として戻ってくるのでしょう。研究では個人の能力ももちろん大切ですが、個人が集まりチームとなることで研究力が何段階も上がっていく、そんなことを強く感じました。研究結果の悲喜こもごもを共有し、気持ちを1つに頑張ってこられた成果が形になる。そんなお話をまるで自分も仲間の一人に加わったような臨場感でお伺いしました。体のほとんどは痛みを感じ、その不快感があるからこそ日常生活を無事に過ごすことが出来る。しかし、痛みについてはまだまだわからないことばかり。また、今回の研究は痛みと関連した触覚やかゆみなどの体性感覚に共通するメカニズムも示唆する。今後も田中先生を中心としたチームの研究に目が離せません。
インタビューアー:研究力向上支援センター特命准教授・URA 上村陽一郎
URA 垣脇成光
【Nature Immunology】: Nature Immunologyは免疫学分野の最高峰の1つに挙げられるNatureの姉妹誌です (外部サイトへリンク)
【プレスリリース】:奈良県立医科大学 研究・産学官連携ページ(皮膚マクロファージによる痛みの調節-新たな鎮痛薬開発の可能性-)
お問い合わせ
公立大学法人奈良県立医科大学 研究力向上支援センター
〒634-8521 奈良県橿原市四条町840番地
電話番号:0744-22-3051
ファックス番号:0744-29-8021
































 〒634-8521 奈良県橿原市四条町840番地
〒634-8521 奈良県橿原市四条町840番地